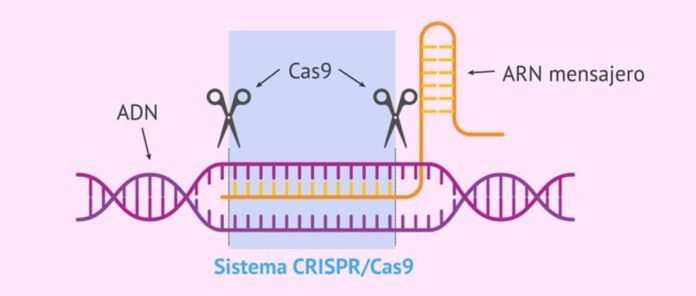
“Sistemas CRISPR-Cas” em bactérias e vírus identificam e destroem sequências virais invasoras. É um sistema imunológico bacteriano e arqueal para proteção contra infecções virais. Em 2012, o sistema CRISPR-Cas foi reconhecido como um genoma ferramenta de edição. Desde então, uma ampla gama de sistemas CRISPR-Cas foi desenvolvida e encontrou aplicações em áreas como terapia genética, diagnóstico, pesquisa e melhoramento de culturas. No entanto, os sistemas CRISPR-Cas atualmente disponíveis têm uso clínico limitado devido a ocorrências frequentes de edição fora do alvo, mutações inesperadas de DNA e problemas hereditários. Pesquisadores relataram recentemente um novo sistema CRISPR-Cas que pode atingir e destruir mRNA e proteínas associados a diferentes doenças genéticas com mais precisão, sem impacto fora do alvo e problemas hereditários. Chamado Craspase, é o primeiro sistema CRISPR-Cas que mostra proteína função de edição. É também o primeiro sistema que pode editar RNA e proteína. Como o Craspase supera muitas limitações dos sistemas CRISPR-Cas existentes, ele tem potencial para revolucionar a terapia genética, o diagnóstico e o monitoramento, a pesquisa biomédica e o melhoramento de culturas.
“Sistema CRISPR-Cas” é o sistema imunológico natural de bactérias e arquéias contra infecções virais que identifica, liga e degrada as sequências do gene viral para proteger. Consiste em duas partes – RNA bacteriano transcrito do gene viral incorporado no genoma bacteriano após a primeira infecção (chamado CRISPR, que identifica as sequências alvo dos genes virais invasores) e um destruidor associado. proteína chamado “CRISPR associado proteína (Cas)”, que liga e degrada as sequências identificadas no gene viral para proteger as bactérias contra vírus.
MAIS BATATA significa “repetições palindrômicas curtas agrupadas regularmente interespaçadas”. É transcrito RNA bacteriano caracterizado por repetições palindrômicas.
As repetições palindrômicas (CRISPRs) foram descobertas pela primeira vez nas sequências de E. coli em 1987. Em 1995, Francisco Mojica observou estruturas semelhantes em archaea, e foi ele quem primeiro pensou nelas como parte do sistema imunológico de bactérias e archaea. Em 2008, foi demonstrado experimentalmente pela primeira vez que o alvo do sistema imunológico de bactérias e arquéias era o DNA estranho e não o mRNA. O mecanismo de identificação e degradação de sequências virais sugeriu que tais sistemas poderiam ser usados como uma ferramenta para edição de genoma. Desde o seu reconhecimento como ferramenta de edição de genoma em 2012, o sistema CRISPR-Cas percorreu um longo caminho como um padrão firmemente estabelecido edição gene sistema e encontrou uma ampla gama de aplicações em biomedicina, agricultura, indústrias farmacêuticas, incluindo terapia genética clínica1,2.
Uma ampla varidade de CRISPR-Os sistemas Cas já estão identificados e atualmente disponíveis para monitoramento e edição de sequências de DNA/RNA para pesquisa, triagem de medicamentos, diagnósticos e tratamentos. Os atuais sistemas CRISPR/Cas são divididos em 2 classes (Classe 1 e 2) e seis tipos (Tipo I a XI). Os sistemas de classe 1 possuem vários Cas proteínas que precisam formar um complexo funcional para se ligar e agir sobre seus alvos. Por outro lado, os sistemas Classe 2 possuem apenas um grande Cas proteína para ligação e degradação de sequências alvo, o que torna os sistemas Classe 2 mais fáceis de usar. Os sistemas Classe 2 comumente usados são Cas 9 Tipo II, Cas13 Tipo VI e Cas12 Tipo V. Esses sistemas podem ter efeitos colaterais indesejados, ou seja, impacto fora do alvo e citotoxicidade3,5.
Terapias genéticas baseados nos atuais sistemas CRISPR-Cas têm uso clínico limitado devido a ocorrências frequentes de edição fora do alvo, mutações inesperadas de DNA, incluindo grandes deleções de fragmentos de DNA e grandes variantes estruturais de DNA em locais no alvo e fora do alvo, o que leva à morte celular e outros problemas hereditários.
Craspase (ou caspase guiada por CRISPR)
Pesquisadores relataram recentemente um novo sistema CRISPER-Cas que é um sistema Cas2-7 Classe 11 Tipo III-E associado a um sistema semelhante a caspase proteína daí nomeado Craspase ou caspase guiada por CRISPR 5 (Caspases são cisteína proteases que desempenham um papel fundamental na apoptose na quebra de estruturas celulares). Tem aplicações potenciais em áreas como terapia genética e diagnóstico. Craspase é guiada por RNA e direcionada a RNA e não se envolve com as sequências de DNA. Pode atingir e destruir mRNA e proteínas associados a diferentes doenças genéticas com mais precisão, sem impacto fora do alvo. Assim, a eliminação de genes associados a doenças é possível por clivagem ao nível do ARNm ou da proteína. Além disso, quando ligado a uma enzima específica, o Craspase também pode ser usado para modificar funções de proteínas. Quando suas funções RNase e protease são removidas, a Craspase é desativada (dCraspase). Não tem função de corte, mas se liga a sequências de RNA e proteínas. Portanto, o dCraspase pode ser usado em diagnósticos e imagens para monitorar e diagnosticar doenças ou vírus.
Craspase é o primeiro sistema CRISPR-Cas que apresenta função de edição de proteínas. É também o primeiro sistema que pode editar RNA e proteínas. Isso é edição gene A função vem com efeitos mínimos fora do alvo e sem problemas hereditários. Portanto, é provável que Craspase seja mais seguro no uso clínico e terapêutico do que outros sistemas CRISPR-Cas atualmente disponíveis. 4,5.
Como o Craspase supera muitas limitações dos sistemas CRISPR-Cas existentes, ele tem potencial para revolucionar a terapia genética, diagnóstico e monitoramento, pesquisa biomédica e melhoramento de culturas. Mais pesquisas são necessárias para desenvolver um sistema de entrega confiável para direcionar com precisão os genes causadores de doenças nas células antes de provar a segurança e a eficácia em ensaios clínicos.
***
Referências:
- Gostimskaya, I. CRISPR–Cas9: Uma história de sua descoberta e considerações éticas de seu uso na edição do genoma. Biochemistry Moscow 87, 777–788 (2022). https://doi.org/10.1134/S0006297922080090
- Chao Li et al 2022. Ferramentas e recursos computacionais para edição do genoma CRISPR/Cas. Genômica, Proteômica e Bioinformática. Disponível online em 24 de março de 2022. DOI: https://doi.org/10.1016/j.gpb.2022.02.006
- van Beljouw, SPB, Sanders, J., Rodríguez-Molina, A. et al. Sistemas CRISPR-Cas direcionados ao RNA. Nat Rev Microbiol 21, 21–34 (2023). https://doi.org/10.1038/s41579-022-00793-y
- Chunyi Hu et al 2022. Craspase é uma protease guiada por RNA CRISPR e ativada por RNA. Ciência. 25 de agosto de 2022. Vol 377, Edição 6612. pp. 1278-1285. DOI: https://doi.org/10.1126/science.add5064
- Huo, G., Shepherd, J. & Pan, X. Craspase: Um novo editor de gene duplo CRISPR/Cas. Functional & Integrative Genomics 23, 98 (2023). Publicação: 23 de março de 2023. DOI: https://doi.org/10.1007/s10142-023-01024-0
***